HPV的简介
德国医学科学家、病毒学家、2008年诺贝尔生理及医学奖获得者 Harald zur Hausen发现了导致宫颈癌的病毒—人乳头瘤病毒(humanpapillomavirus,HPV),并致力于研究人乳头状瘤病毒与宫颈癌之间关系。
HPV是无包膜的具有嗜上皮性的双链环状DNA病毒(长度约8000bp),病毒由核酸和衣壳蛋白组成,核酸可分为3个基因组区域,约10个开放阅读框(open reading frame,ORF):早期编码区(E区:E1、E2、E4、E5、E6和E7)编码非结构蛋白;晚期编码区(L区:L1和L2)编码病毒粒子和病毒传播所需的结构蛋白,长调控区(longcontrolregion,LCR)—含有早期启动子、调控病毒和细胞蛋白转录的调控位点。
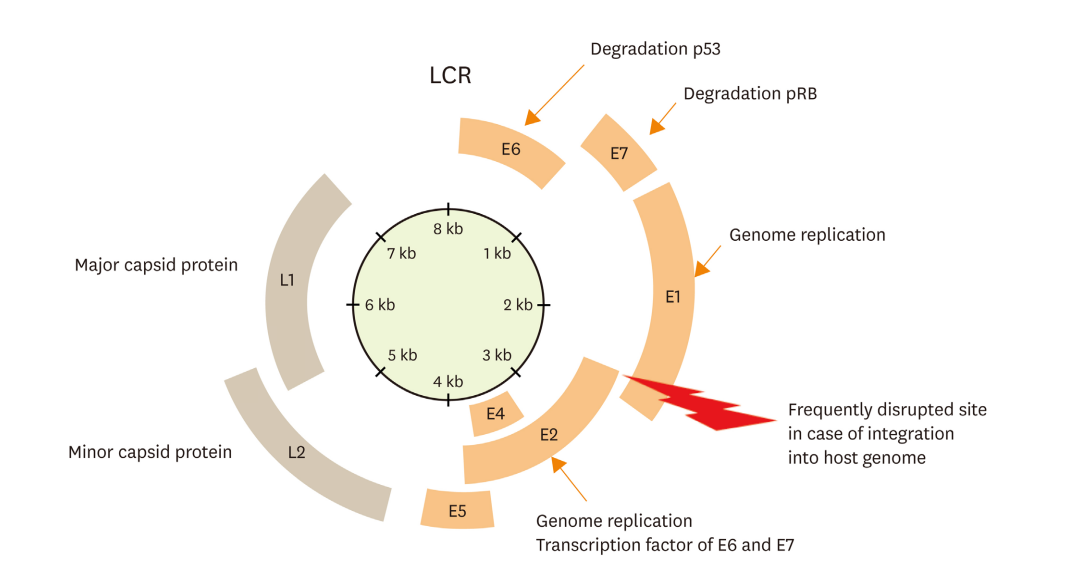
图1 HPV基因组结构
目前已鉴定了200多种HPV基因型别,按照临床表现可分为低危型HPV和高危型HPV。据“宫颈癌诊疗指南(2022年版)”,高危型(如 HPV16、18、31、33、35、39、45、51、52、56、58、59、68 型)与子宫颈癌、阴茎癌、外阴癌、肛门癌和阴道癌以及头颈部鳞状细胞癌(口腔癌、口咽癌和喉癌)的发生相关,尤其是HPV16型和18型和子宫颈癌关系最为密切。子宫颈癌是常见的妇科恶性肿瘤之一,发病率在我国女性恶性肿瘤中居第二位,位于乳腺癌之后。低危型 HPV(如6、11、42、43、44 型)感染则可能引起生殖器及肛周湿疣。据“中国尖锐湿疣临床诊疗指南”,90%~95%的尖锐湿疣病例是由低危型病毒 HPV6型和11型引起的。统计数据显示,高危HPV感染所引起的癌症发病人数约占全球癌症中发病率的5%。国际癌症研究协会(IARC)认定持续性高危型 HPV 感染正是诱发宫颈癌的重要原因,99%以上的宫颈癌与HPV感染有关。研究结果显示75%以上宫颈癌中 HPV16、18、31和45型呈阳性,而HPV16和HPV18型约引起70%左右的宫颈癌。宫颈癌是目前病因明确,可以早期预防,有望被消灭的一种癌症。
HPV感染和相关疾病的进展
HPV病毒具有嗜上皮特性,其感染宿主后,在表皮、生殖器、口腔黏膜等部位的上皮基底细胞中大量复制,当机体免疫力降低后可随机整合到宿主基因组中,随后沉默E2基因,从而减少其对E6、E7基因的抑制,使E6、E7蛋白过表达,辅以E5蛋白的表达,从而诱导感染细胞无限增殖甚至癌变。
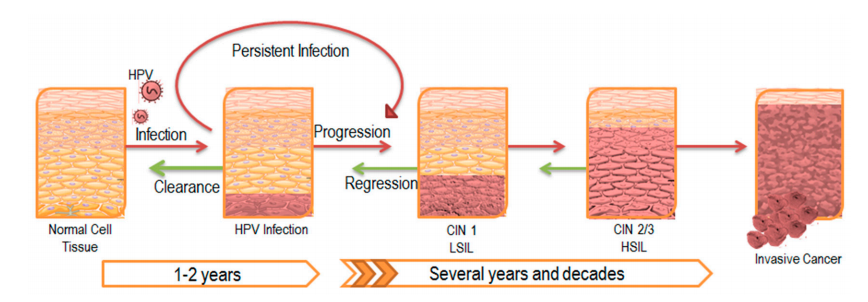
图2 HPV感染疾病进展
在HPV感染人群中有10-20%的感染是潜伏存在的,进而导致疾病进展。由此产生的病变也被称为中枢上皮内瘤变(CIN),并根据其严重程度进行分类。最终,低级别鳞状上皮内病变(LSIL)发展为高级别鳞状上皮内病变(HSIL),最终导致浸润性癌。尽管肿瘤在初始治疗后有所消退,但大多数潜伏感染病例阻止了病毒感染的完全清除,最终导致病变复发。30岁以上妇女HPV持续感染平均8-24个月可发生宫颈癌前病变,平均8-12年可发展为浸润癌。
HPV感染的预防与治疗
接种HPV疫苗是预防HPV感染及宫颈癌的有效手段。然而,接种疫苗对先前存在的HPV感染和相关恶性肿瘤并无治疗效果。开发前瞻性治疗方法以降低与HPV有关的全球癌症发病率和死亡率是目前最紧迫的健康需求。
目前临床常用治疗HPV的主要方法包括:重组人干扰素α-2b外用剂型(包括:栓剂、阴道泡腾胶囊(片)、凝胶、软膏剂等)、中药制剂及抗HPV生物蛋白敷料。干扰素以及中药制剂等通过调节机体免疫功能等机制发挥抗病毒作用。
乳头状瘤病毒(PV)动物模型
HPV感染机制探索及防治策略研究需要合适的动物模型,由于病毒的宿主特异性,尚未建立理想的HPV感染动物模型。目前的动物模型主要为动物乳头状瘤病毒(PV)感染其天然宿主的皮肤和黏膜而建立的,主要包括兔PV感染兔的皮肤感染模型、犬口腔PV感染狗的黏膜感染模型、牛PV感染牛的黏膜感染模型。这些动物PV感染模型不能完全模拟HPV与宿主的相互作用关系,仅为HPV的感染机制研究提供参考。HPV感染动物模型的缺乏,给HPV感染性疾病的研究、HPV疫苗和药物的体内效果评价等造成困难。
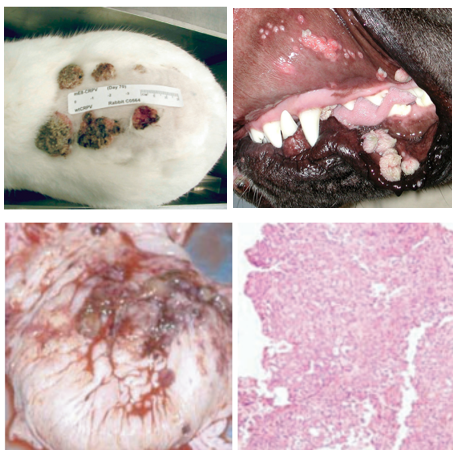
图3 乳头瘤病毒动物模型
棉尾兔乳头瘤皮肤感染模型Antivir Chem Chemother.2005,16(6):355-62.、犬乳头瘤感染狗的黏膜模型Vet J. 2017,225:23-31.、牛乳头瘤感染牛的黏膜模型Vet Res. 2008,39(5):45.
人HPV假病毒感染小鼠模型
武汉班科生物技术有限公司研发团队利用基因工程技术构建了人HPV假病毒粒子(PsV)并成功建立了小鼠感染模型。HPV PsV由病毒衣壳蛋白(L1和L2)和内部取代病毒基因组的报告基因组成,其优点在于能快速的生产大量病毒样颗粒,而携带的报告基因则便于病毒定量检测。HPV PsV可成功感染经诱导损伤的小鼠阴道组织,可以用于小分子、抗体等的抗病毒药效评价,以及疫苗的保护效果评价。该动物模型操作安全、周期短、结果准确可定量,能够有效降低研发成本,大大加速药物和疫苗的研发进度,体现出公司团队过硬的研发实力。
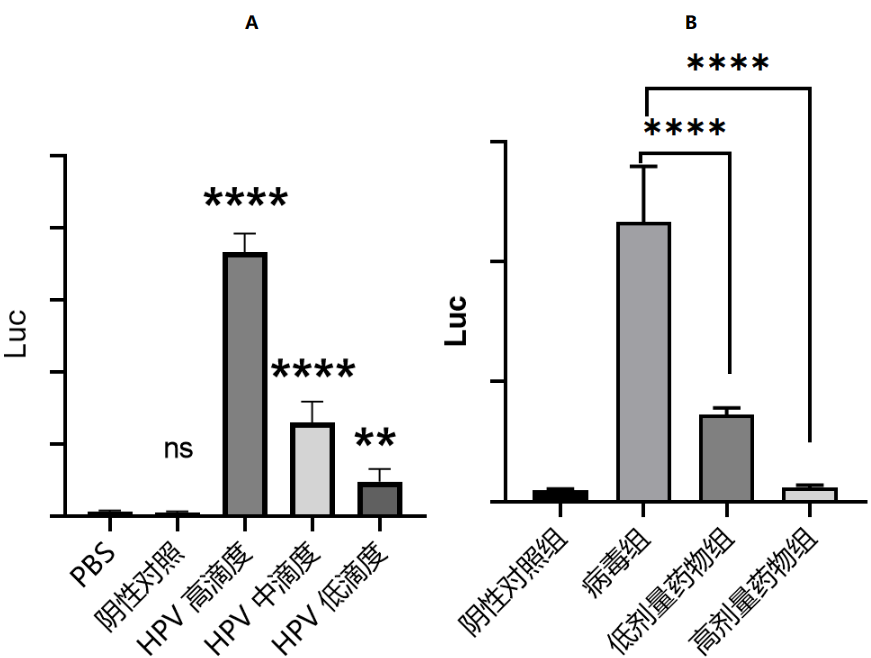
图4 HPV假病毒感染小鼠实验结果
A. 不同剂量HPV PsV感染小鼠;B. 药物抗HPV感染效果。
技术合作请咨询
电话:027-87806108
邮箱:zhangzhe@bankbiotech.com、liuchunlan@bankbiotech.com
参考文献:
[1] Lee SJ, Yang A, Wu TC, Hung CF. Immunotherapy for human papillomavirus-associated disease and cervical cancer: review of clinical and translational research. Journal of Gynecologic Oncology. 2016, 27(5):e51.
[2] Shanmugasundaram S, You J. Targeting Persistent Human Papillomavirus Infection. Viruses. 2017, 9(8):229.
[3] Culp TD, Cladel NM, Balogh KK, Budgeon LR, Mejia AF, Christensen ND. Papillomavirus particles assembled in 293TT cells are infectious in vivo. J Virol. 2006,80(22):11381-4.
[4] Bravo IG, Félez-Sánchez M. Papillomaviruses: Viral evolution, cancer and evolutionary medicine. Evol Med Public Health. 2015,2015(1):32-51.
[5] Rector A, Van Ranst M. Animal papillomaviruses. Virology. 2013, 445(1-2):213-23.
[6] chlecht N F , Platt R W , Eliane D F ,et al.Human papillomavirus infection and time to progression and regression of cervical intraepithelial neoplasia.[J].Journal of the National Cancer Institute, 2003, 95(17):1336-1343.
[7] Nie, J., Wu, X., Ma, J. et al. Development of in vitro and in vivo rabies virus neutralization assays based on a high-titer pseudovirus system. Sci Rep 7, 42769 (2017).
[8] Biryukov J, Meyers C. Papillomavirus Infectious Pathways: A Comparison of Systems. Viruses. 2015 Aug 4;7(8):4303-25.



